医学院那洁课题组开发人多能干细胞向血管细胞高效分化体系
清华新闻网4月2日电 近日,清华大学医学院那洁课题组发表学科交叉论文,揭示心血管前体细胞分化新机理,创建了省略胰岛素的培养体系,用于高效分化获得血管内皮细胞和平滑肌细胞,最后在血管损伤缺血动物模型进行细胞移植实验治疗,证实这些细胞具有良好的在体内形成血管的能力。这一研究为血管重建、治疗组织器官缺血提供可能的细胞来源。
心血管疾病,包括缺血性疾病是造成我国成年人死亡的最主要因素之一。由人多能干细胞分化来的血管细胞(主要为内皮细胞和平滑肌细胞)具有治疗这些疾病的应用前景,但目前采用的分化系统存在成分复杂、成本高和无法大量产生细胞等缺点。本研究通过使用不含胰岛素的AATS分化体系,实现了用最简化的培养成分高效分化血管内皮细胞和平滑肌细胞(图1),并通过细胞移植验证了这些细胞在动物模型体内的血管重建功能。
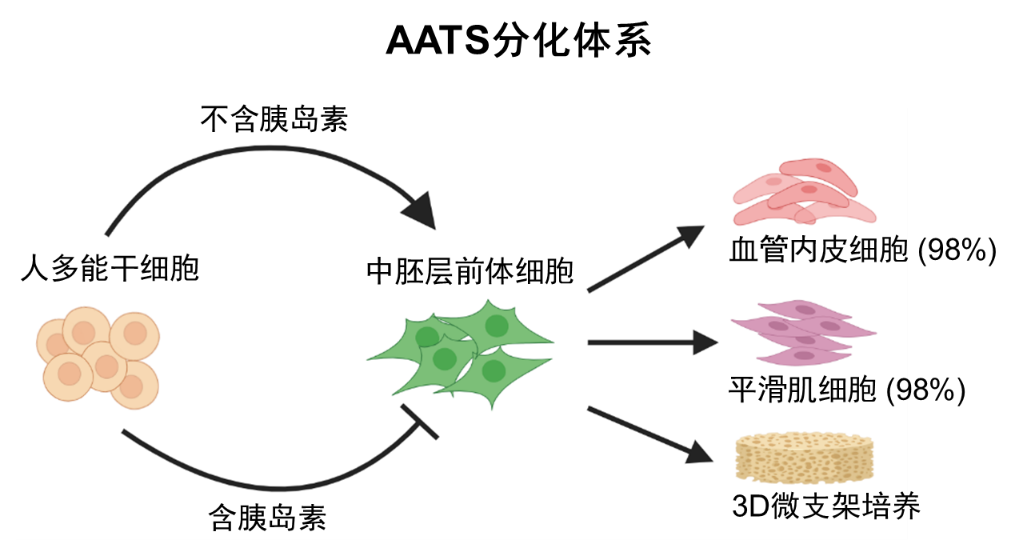
图1.不含胰岛素的AATS体系可以促进中胚层和血管内皮细胞及平滑肌细胞高效分化
本研究发现胰岛素会抑制心血管中胚层细胞的诱导,进而抑制内皮细胞的产生。省略胰岛素使细胞迅速向氧化磷酸化的代谢方式转变、加强细胞的自噬活动及开放中胚层基因所在染色质区域,从而促进中胚层细胞高效诱导。在无胰岛素的培养液中,可以高效获取血管内皮细胞(98%)和平滑肌细胞(98%)。这些血管细胞可在体外形成管状结构,响应刺激和收缩,且具有低免疫原性。此外,结合3D材料微支架培养,该分化体系可以实现长期大量分化血管内皮细胞。最后,将分化的细胞移植到下肢缺血和大脑中动脉缺血小鼠模型,修复或逆转了这些模型小鼠因缺血导致的下肢坏死和偏瘫,实现了缺血部位的血管重建和对神经组织的保护(图2)。
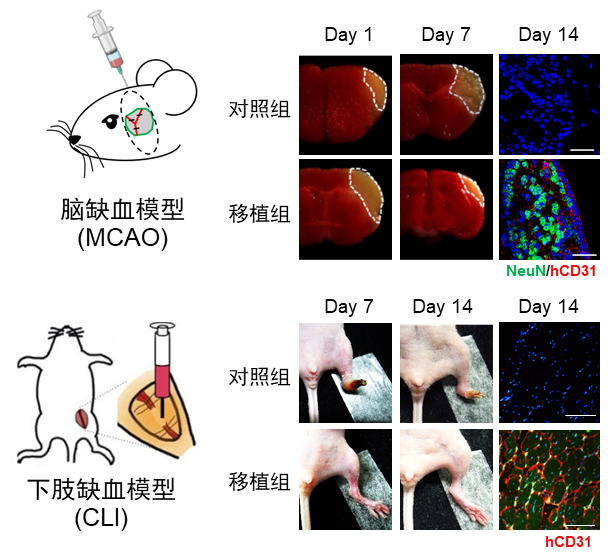
图2. AATS体系分化得到的血管细胞可以用于小鼠缺血部位血管再生和损伤修复
综上,本研究阐明了胰岛素对心血管中胚层细胞诱导的抑制机理,开发了成本较低、成分简单的血管细胞高效分化系统。为实现体外大量获得血管细胞提供了新的方法,具有潜在的临床应用与转化前景。
该研究已于2月份发表在《生物材料》(Biomaterials)杂志,题目为“一套简化的不含胰岛素的培养体系用于人多能干细胞高效分化内皮细胞和平滑肌细胞”(Efficient endothelial and smooth muscle cell differentiation from human pluripotent stem cells through a simplified insulin-free culture system)。清华大学医学院那洁副教授为该论文通讯作者,医学院已毕业博士生张凤枝、博士研究生朱咏林和博士后陈静为本文共同第一作者。清华大学药学院陈立功研究员、博士生匡文华对本研究中代谢组样品制备和数据分析提供了大力帮助和指导。清华大学长庚医院张家宁教授对本研究中小鼠缺血模型的构建提供了重要的指导。此外,医学院生物医学工程系杜亚楠教授和李雅倩博士提供了3D组织工程微支架。那洁实验室博士生黄如金、段福宇、邱辉和科研助理明佳等也对本研究作出了重要贡献。
本研究由国家干细胞及转化研究重点专项、国家自然科学基金委项目、清华-北京大学联合生命科学中心、蛋白质研究技术中心、结构生物学高精尖创新中心等提供经费和测试仪器支持。
供稿:医学院
编辑:李华山
审核:李晨晖
【免责申明】本专题图片均来源于学校官网或互联网,若有侵权请联系400-0815-589删除。