中南大学梁德生团队在血友病A基因编辑治疗领域取得重要进展
近日,中南大学生命科学学院医学遗传学研究中心梁德生课题组在国际顶级期刊Signal Transduction and Targeted Therapy在线发表血友病A基因编辑治疗新策略的研究成果,文章题为“Targeted B-domain deletion restores F8 function in human endothelial cells and mice”(《靶向缺失F8基因B区编码序列恢复功能性FVIII表达》)。
血友病A(hemophilia A, HA)是最常见的遗传性凝血功能障碍疾病,在男性中发病率约为1/5000,至今尚无根治方法。基因治疗有望治愈血友病。HA由F8基因突变致功能性的凝血因子VIII(FVIII)缺乏而引起。F8基因长达186kb,是已克隆的最大基因之一,目前基于AAV的基因添加策略受限于装载量小、免疫原性问题及潜在插入突变风险,基因编辑治疗可望克服这些瓶颈。FVIII包括3个A区,1个B区和2个C区结构域,有15-26%的重型HA患者致病突变发生B区编码序列(F8-B)中,B区占FVIII总长的39%,但发挥凝血功能的FVIII并不包含B结构域。课题组基于FVIII结构分析与前期研究基础提出一种可覆盖F8-B内全部致病突变的“通用型”原位基因编辑治疗策略:靶向缺失F8-B从而恢复功能性FVIII表达。在F8-B移码突变的重型HA病人诱导多能干细胞(HA-iPSCs)中,在F8基因原位靶向缺失F8-B。基因编辑后HA-iPSCs分化的内皮祖细胞(iEPCs)和内皮细胞(iECs)中FVIII的表达、分泌与活性均得到恢复,移植iEPCs显著改善模型小鼠的出血表型。
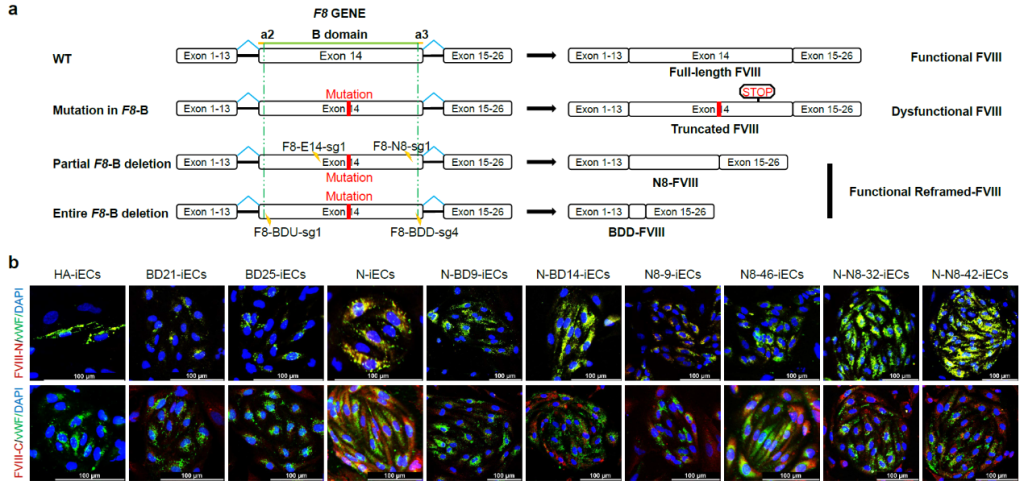
基因修复后iECs内FVIII表达得到修正
该研究首次在F8原位实现F8-B的靶向缺失,并应用于HA基因治疗研究,为所有F8-B突变的HA患者提供一种通用且高效的基因疗法。同时,在国际上首次证明F8-B靶向缺失的内源性FVIII具有凝血功能,为重组B区缺失型FVIII的临床应用和B区缺失F8基因治疗研究提供理论依据。
梁德生教授团队在遗传病的基因治疗研究方面取得了系列原创成果,其中“基因修正血友病A病人iPSCs来源的ECs治疗研究”获法国国家血浆制品集团(LFB)资助进行FDA临床试验申请的前期效果评估;“靶向基因修饰干细胞治疗”目前已进入临床转化阶段。
中南大学博士后胡志青为论文第一作者,梁德生教授和周妙金博士为共同通讯作者,中南大学生命科学学院为唯一完成单位。该研究得到了国家重点研发项目、国家自然科学基金项目、中国博士后科学基金第2批特别资助、湖南省自然科学基金项目的支持。
【免责申明】本专题图片均来源于学校官网或互联网,若有侵权请联系400-0815-589删除。